Оздоровление перспективных сортов картофеля с применением комбинированной терапии в культуре in vitro

Современный картофель (S. tuberosum ssp. tuberosum L.) представляет собой тетраплоид, полученный путем продолжительной селекции интродуцированного в Европе культивируемого картофеля Andigena (S. tuberosum ssp. andigena). Одну из наиболее серьезных угроз для сельского хозяйства и экономики в целом (как в России, так и за рубежом) представляют фитовирусы. Урожайность и качество картофеля зависят от степени его зараженности патогенами, включая бактерии, грибы, вирусы и вироиды. Вирусная инфекция способна наносить этой продовольственной культуре значительный ущерб.
В результате многолетней селекционной работы созданные сорта картофеля являются носителями фитопатогенов в латентной форме, которые передаются клоновому потомству. Освобождение семенного материала от вирусных инфекций и сохранение высокопродуктивных качеств новых сортов обеспечиваются соблюдением системы безвирусного семеноводства картофеля. Реализация утвержденной Правительством России Подпрограммы «Развитие селекции и семеноводства картофеля в Российской Федерации» предусматривает повышение урожайности картофеля за счет создания и быстрого продвижения новых высокопродуктивных сортов в производство на основе современных технологий выращивания качественного семенного материала.
Производство семенного картофеля в России регламентировано ГОСТ 33996–2016 и ГОСТ Р 59551-2021, которые предусматривают технические условия получения и воспроизводства посадочного материала картофеля и применение методов диагностики фитопатогенов картофеля. В данных нормативных документах отмечается, что семенной картофель должен быть свободен от:
- вируса скручивания листьев картофеля, ВСЛК (potato leaf roll virus, PLRV);
- Y вируса картофеля, YВК (Potato virus Y, PVY);
- X вируса картофеля, ХВК (Potato virus X, PVX);
- S вируса картофеля, SBK (Potato virus S, PVS);
- M вируса картофеля, МВК (Potato virus M, PVM).
Для получения достаточного количества качественного семенного материала картофеля, свободного от вирусов, существуют способы оздоровления с применением различных биотехнологических методов элиминации вирусов в культуре in vitro, которые непрерывно усовершенствуются исследователями. Культура меристем используется отдельно или в сочетании с термо-, электро-, крио- и химиотерапией. Сотрудниками ФГБНУ «ФИЦ картофеля им. А.Г. Лорха» (Красково, Московская обл., Россия) разработан новый способ оздоровления сортов картофеля, основанный на применении термотерапии микрорастений с последующим вычленением из них меристем, который существенно сокращает время на проведение работ по оздоровлению и обеспечивает круглогодичный выход здорового in vitro материала.
Элиминация вируса картофеля в значительной степени зависит от сорта картофеля, противовирусных средств, типа вируса, продолжительности термической обработки. Приемы антивирусной терапии неодинаковы по эффективности, а в ряде случаев одни и те же подходы в разных лабораториях дают противоречивые результаты.
Таким образом, разработка способов оздоровления растений картофеля от вирусных инфекций остается крайне актуальной.
Цель исследования — разработать эффективную схему комплексной антивирусной термохимиотерапии оздоровления растений картофеля от вирусной инфекцииin vitro с использованием в безвирусном семеноводстве.
Материалы и методы исследования
В качестве объекта исследования был взят перспективный сорт картофеля Посейдон (селекционный № При-14-36-3), полученный в ФГБНУ «ФНЦ агробиотехнологий Дальнего Востока им. А.К. Чайки» (Уссурийск, Приморский край, Россия). Полевые растения из питомника конкурсного испытания в количестве 20 шт. анализировали на присутствие вирусов PVX, PVY, PVA, PVS, PVM и PLRV методом иммуноферментного анализа в испытательной лаборатории диагностики болезней картофеля, уполномоченной в Системе добровольной сертификации «Россельхозцентр». Проростки исходных клубней и микрорастения на скрытую зараженность вирусами тестировали методом RT-PCR. Тотальную РНК выделяли коммерческими наборами для нуклеиновых кислот из растительного материала «ФитоСорб» (ООО «НПК “Синтол”», Россия) с использованием магнитных частиц на автоматической станции выделения KingFisher Duo Prime (Thermo Fisher Scientific, Сингапур). Эффективность выделения определяли методом электрофореза в 1%-ном агарозном геле, окрашенном бромистым этидием, с последующей визуализацией облучением ультрафиолетом в гель-документирующей системе GelDoc Go (BioRad, USA). Наличие/отсутствие фитовирусов в пробах проводили одношаговой ОТ-ПЦР с флуоресцентной детекцией в реальном времени в амплификаторе Applied Biosystems QuantStudio 5 RealTime PCR Instrument (Thermo Fisher Scientific, Сингапур) с использованием коммерческих наборов серии «Фитоскрин» Potato Virus X. Y. M. L. S. A – РВ (ООО «НПК “Синтол”», Россия), предназначенных для выявления вирусов PVХ, PVY, PVM, PLRV, PVS, PVA.
В процессе оздоровления совмещали метод культуры ткани с комбинированной антивирусной термохимиотерапией микрорастений, применяя противовирусный препарат рибавирин (30 мл/л). В культуру in vitro изолировали верхушечные (апексы) и пазушные почки крупного (2–4 мм) размера, взятые от клубней с наименьшей вирусной нагрузкой. Для введения в культуру использовали этиолированные ростки. Первичные экспланты культивировали на питательной среде с минеральной основой по Мурасиге и Скугу (МS) модифицированного состава (мг/л): тиамин — 0,5, пиридоксин — 0,5, аскорбиновая кислота — 0,5, гидролизат казеина — 50, мезоинозит — 80, сахароза – 20 000, агар — 6000, рибавирин — 30.
Культивирование пробирок с эксплантами проводили в климатической камере MLR-352H (Sanyo, Япония) при температуре плюс 23 ± 1 °C, освещенности 4 клк, световом дне 16 ч., влажности воздуха 60–70%. Микроклоны картофеля выращивали в культуральной комнате на фитостеллажах со светодиодным освещением серии X-bright Fito (ООО «ЭЛСИС БелГУ», Россия) и фитостеллажах с люминесцентными лампами белого света в сочетании с фитолампами (ООО «AВТех», Россия) при освещенности 4,5–5 клк, температуре плюс 22 ± 3 °С, 16-часовом световом дне, влажности воздуха 60–70%.
Результаты и обсуждение
В результате диагностики 20 растений сорта картофеля Посейдон, находящихся в питомнике конкурсного сортоиспытания, методом ИФА выявлены и отобраны три клона с наименьшей вирусной нагрузкой (№ 2, 3, 10). Данные образцы содержали комплекс вирусов PVY, PVS, PVM и PLRV, при этом установлено отсутствие вирусов PVX и PVA (табл. 1).
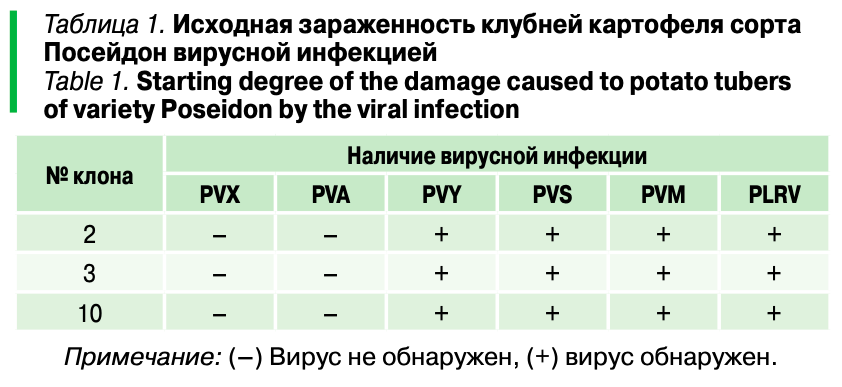
В связи с этим, в процедуру по оздоровлению в культуре in vitro были взяты три ранее отобранных клона, которые отличились минимальным содержанием вирусов. Далее асептические экспланты трех клонов картофеля (№ 2, 3, 10) изолировали в культуру in vitro на питательную среду с антивирусным препаратом рибавирин в концентрации 30 мг/л.
Комбинированная терапия включала три этапа общей продолжительностью 150 дней, на каждом из которых экспланты и микропобеги картофеля пассировали на питательную среду МS с рибавирином (30 мг/л):
1-й этап — введение и культивирование первичных эксплантов на питательной среде МS с добавлением рибавирина (30 мг/л) при 23 ± 1 °C в течение 50 дней;
2-й этап состоял из нескольких последовательных циклов:
• пассирование микропобегов на питательную среду с рибавирином (30 мг/л) и культивирование в течение 36 дней при 23 ± 1 °C;
• культивирование микропобегов в климатической камере с последовательным повышением температуры с 23 до 38 °C и выдерживание в течение 14 дней при 38 °С;
• культивирование микропобегов при 23 ± 1 °C в течение 10 дней;
3-й этап — черенкование и культивирование микрорастений на среде МS с добавлением рибавирина (30 мг/л) при 23 ± 1 °C в течение 30 дней.
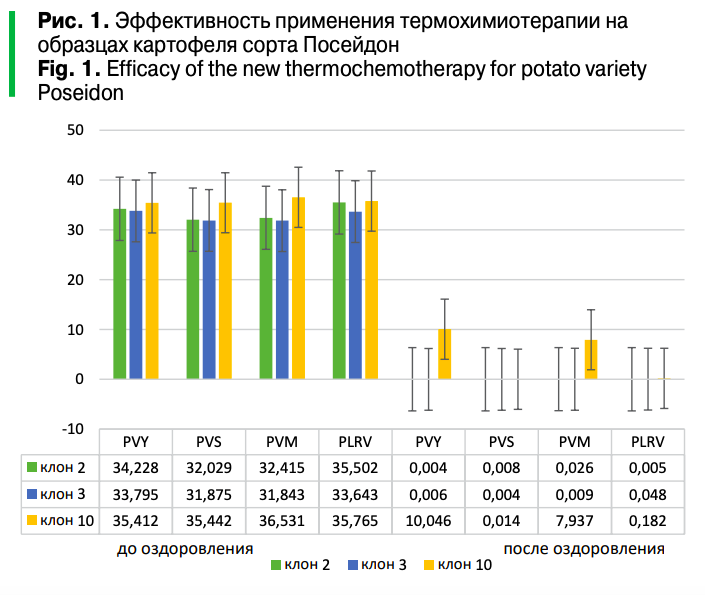
В процессе выполнения работы проводили ПЦР-диагностику растительного материала на наличие вирусов. Микрорастения картофеля с полным отсутствием вирусной инфекции после проведения антивирусной термохимиотерапии удалось получить только для двух клонов (№ 2, 3). Полная элиминация вирусов PVS и PLRV и частичная элиминация PVY и PVM были отмечены для клона № 10 (рис. 1).
Выводы
Для получения оздоровленных растений перспективного сорта картофеля Посейдон и ингибирования комплексной инфекции вирусов PVY, PVS, PVM, PLRV разработана эффективная схема комплексной термохимиотерапии общей продолжительностью 150 дней, включающая три последовательных цикла выращивания in vitro растений на среде Мурасиге и Скуга (МS) с рибавирином (30 мг/л) при одновременном воздействии повышенной температуры (38 °С) на микропобеги картофеля в течение 14 дней. В результате проведенных работ, применив разработанную схему, получены оздоровленные растения картофеля сорта Посейдон, которые включены в процесс безвирусного семеноводства ФГБНУ «ФНЦ агробиотехнологий Дальнего Востока им. А.К. Чайки».
Об авторах
Елена Васильевна Шищенко, младший научный сотрудник лаборатории сельскохозяйственной биотехнологии,
chagovec75@mail.ru; https://orcid.org/0000-0002-1204-0515
Елена Николаевна Барсукова, кандидат сельскохозяйственных наук, ведущий научный сотрудник лаборатории сельскохозяйственной биотехнологии,
enbar9@yandex.ru; https://orcid.org/0000-0001-7880-252X
Ирина Вячеславовна Ким, кандидат сельскохозяйственных наук, ведущий научный сотрудник отдела картофелеводства,
kimira-80@mail.ru; https://orcid.org/0000-0002-0656-0645
Ольга Абдулалиевна Собко, аспирант, научный сотрудник лаборатории селекционно-генетических исследований полевых культур,
o.eyvazova@gmail.com; https://orcid.org/0000-0002-4383-3390
Алена Сергеевна Чибизова, младший научный сотрудник лаборатории сельскохозяйственной биотехнологии,
chibizova1991@bk.ru; https://orcid.org/0000-0003-2160-5589
Федеральный научный центр агробиотехнологий Дальнего Востока им. А.К. Чайки, ул. Воложенина, 30, пос. Тимирязевский, Уссурийск, Приморский край, 692539, Россия
УДК 635.21:631.533:581.143.6 DOI: 10.32634/0869-8155-2023-374-9-116-119
Сельское хозяйство, ветеринария, зоотехния, агрономия, агроинженерия, пищевые технологии





















